El Zinc como Metal Protector
De Construmatica
Revisión del 08:18 1 dic 2008 de imported>Monylit (→Enlaces Externos)

|
Nota: Este artículo ha sido creado gracias a APTA en el marco del Programa de Afiliados de la Construpedia. El contenido está disponible en el sitio web de APTA.
¡Atención! Esté artículo está sujeto a Derecho de Autor. |
|---|
El Zinc Como Metal Protector
La protección catódica, diferencia fundamental respecto a otros revestimientos barrera.
Dos invenciones ya antiguas, han sido la base de un procedimiento de protección del acero frente a la corrosión de notable eficacia, cuya utilización y tecnología no ha dejado de desarrollarse en el transcurso de los años. Fue en 1742 cuando el químico francés Malouin demostró que la inmersión del acero en zinc fundido proporcionaba un recubrimiento protector de la corrosión de gran eficacia.
Los posteriores desarrollos Stanislaus Sorel y la puesta a punto en 1836 de un procedimiento económico para decapar el acero, abrieron la puerta la utilización industrial de este nuevo procedimiento de protección del acero:
La galvanización en caliente.
Fue el propio Sorel quien puso de manifiesto el efecto de protección galvánica, que proporcionan estos recubrimientos de zinc.
Había descubierto la protección catódica o de sacrificio.
Por este motivo empleó el término galvanisation en su patente francesa presentada en Julio de 1837.
Hoy día sabemos que la corrosión de la mayoría de los metales en el medio ambiente es un fenómeno de naturaleza electroquímica, que necesita de humedad y oxígeno para que pueda desarrollarse.
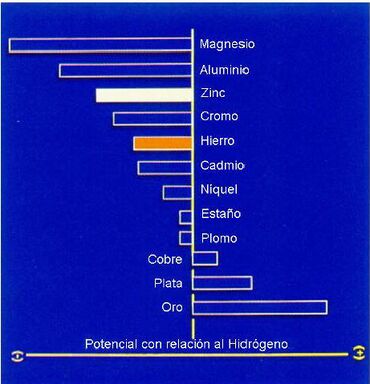
Una medida de la tendencia a la corrosión de los metales en su potencial normal y la ordenación de los metales de conformidad con sus potenciales normales constituye la serie galvánica de los metales que se muestra de forma simplificada en la figura siguiente:
Los metales situados por encima del hierro en esta tabla, como es el caso del zinc, se denominan anódicos con respecto al hierro.
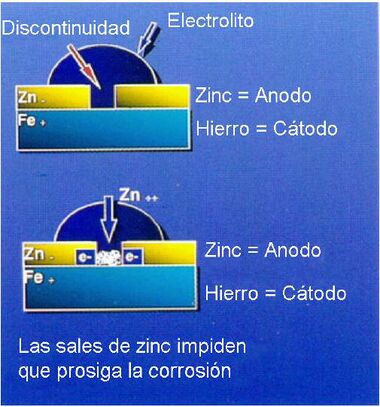
Ésto significa que puestos en contacto con el hierro, constiuirán el ánodo de la pila de corrosión que puede formarse en presencia de humedad y oxígeno y será en este anodo en donde se experimente la oxidación, mientras que el hierro, que constituirá la parte catódica de dicha pila, permanecerá inalterado.
Este es el fundamento de la Protección Catódica o de Sacrificio.
Los recubrimientos de zinc ejercen una activa protección catódica sobre las piezas y elementos de hierro y acero sobre los que se aplican, pudiéndose asegurar que mientras exista zinc remanente sobre la superficie de dichas piezas el acero base de las mismas permanecerá inalterado.
Por otra parte, los recubrimientos de zinc proporcionan al acero una protección de tipo barrera muy eficaz, debido a que con la humedad y el anhídrido carbónico del aire el zinc forma sobre su superficie una capa de pasivación autoprotectora de carbonatos básicos de zinc muy insoluble, compacta y adherente y que es la causa de que la velocidad de corrosión del zinc sea de 10 a 30 veces inferior a la del acero.
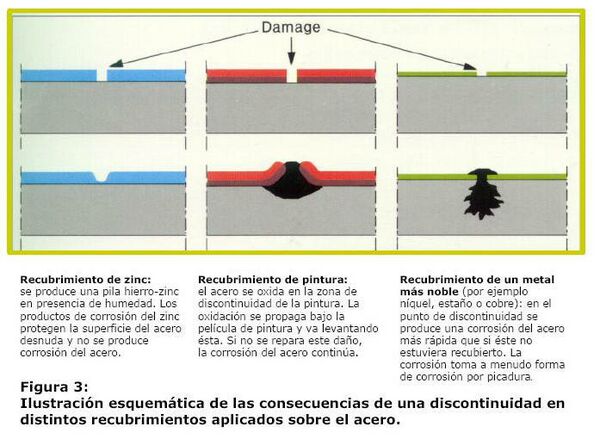
Debido al efecto de protección catódica, en las piezas de acero protegidas con recubrimientos de zinc, no se oxidan las pequeñas zonas desnudas del recubrimiento que puedan producirse como consecuencia de golpes o rozaduras durante el transporte o montaje de las piezas (ver el gráfico sobre estas líneas). Estas zonas desnudas sí son motivo de preocupación y deben restaurarse en el caso de los recubrimientos que protegen únicamente por efecto barrera, como es el caso de la mayoría de las pinturas.
Mayor atención debe prestarse todavía a los defectos que se produzcan en los recubrimientos de metales más nobles que el acero (situados por debajo del hierro en la serie galvánica de los metales), puesto que en las zonas desnudas de estos recubrimientos se focalizará la corrosión del acero con una intensidad mucho mayor que si éste estuviera sin proteger, tomando frecuentemente en este caso forma de corrosión por picaduras que pueden afectar a la integridad estructural del material. Ver gráfico siguiente: